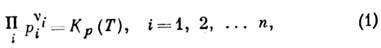
Диссоциативное равновесие - состояние газа (или разбавленного раствора), в к-ром имеет место равенство
скоростей реакций распада (диссоциации) молекул и обратных реакций их воссоединения
(рекомбинации) из атомов и(или) радикалов. Понятие о Д. р. используется преим.
в астрофизике, где обычно приходится иметь дело с гомогенной газовой средой.
Д. р. является частным выражением понятия химического равновесия.
В газе, состоящем из п компонентов, образованных т хим. элементами, может протекать п-т независимых реакций, т. е. реакций, не сводимых к линейным комбинациям др.
реакций. Систему независимых реакций образуют, в частности, реакции диссоциации
всех входящих в газовую смесь молекул на составляющие их атомы. Условие хим.
равновесия - равенство скоростей
прямых и обратных реакций - может быть выражено в виде действующих масс закона, записанного для каждой из независимых реакций:
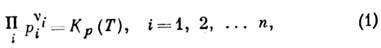
где pi - парциальные давления компонентов, 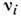 -их
стехиометрия, коэф., Кр - константа хим. равновесия (константа
диссоциации), зависящая только от температуры T. Величина Кр определяется изменением энергии Гиббса в результате реакции:
-их
стехиометрия, коэф., Кр - константа хим. равновесия (константа
диссоциации), зависящая только от температуры T. Величина Кр определяется изменением энергии Гиббса в результате реакции:
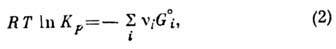
где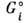 -
энергия Гиббса i-гo компонента, R - универсальная газовая постоянная.
Значок ° означает, что соответствующая величина определена для вещества
в стандартном состоянии. Стандартным состоянием для газообразного вещества при
данной температуре T является состояние гипотетич. идеального газа с температурой
T при давлении р=1 атм. Поскольку
-
энергия Гиббса i-гo компонента, R - универсальная газовая постоянная.
Значок ° означает, что соответствующая величина определена для вещества
в стандартном состоянии. Стандартным состоянием для газообразного вещества при
данной температуре T является состояние гипотетич. идеального газа с температурой
T при давлении р=1 атм. Поскольку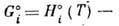
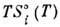 , где
, где 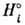 -энтальпия
i-гo компонента,
-энтальпия
i-гo компонента, 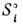 -
его энтропия, то:
-
его энтропия, то:
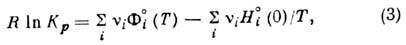
где 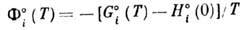 -т. н. приведённая энергия Гиббса, к-рая может быть вычислена, если известна
полная статистич. сумма Qi для соответствующего компонента
-т. н. приведённая энергия Гиббса, к-рая может быть вычислена, если известна
полная статистич. сумма Qi для соответствующего компонента
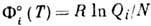 , где N
- число Авогадро. Величины
, где N
- число Авогадро. Величины 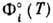 рассчитаны для мн. веществ. Для вычисления
рассчитаны для мн. веществ. Для вычисления 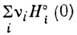 используются приводимые в справочниках величины
используются приводимые в справочниках величины 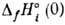 -энтальпии
образования веществ из элементов в стандартных состояниях при Т=0 К;
в соответствии с законом Гесса:
-энтальпии
образования веществ из элементов в стандартных состояниях при Т=0 К;
в соответствии с законом Гесса:
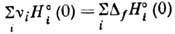
Существует неск. способов
отыскания равновесного хим. состава газа с помощью констант диссоциации независимых
реакций. Часто используется метод, в к-ром сначала определяют парциальные давления
свободных атомов. Для этого составляется m ур-ний баланса массы:
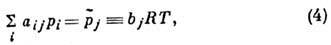
где 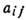 - число атомов элемента j в молекуле сорта i, рi - парциальное давление этих молекул, bj - полное число
молей элемента j в смеси,
- число атомов элемента j в молекуле сорта i, рi - парциальное давление этих молекул, bj - полное число
молей элемента j в смеси, 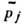 -
"фиктивное" давление элемента j, т. е. то парциальное давление
соответствующих свободных атомов, к-рое имело бы место при полной диссоциации
всех содержащих данный элемент молекул. С помощью соответствующих констант диссоциации
давление рi в ур-ниях (4) может быть выражено через парциальные
давления рj составляющих элементов, находящихся в свободноатомном
состоянии. В результате из (4) получим систему нелинейных алгебраич. ур-ний
для pj. Определив из этой системы все pj, можно
вычислить рi для любого интересующего нас сорта молекул, составляя
соответствующие ур-ния диссоциации (1). При расчётах Д. р. качественный состав
газовой смеси должен быть задан заранее, и от исследователя требуется определ.
интуиция, чтобы не упустить важных соединений, к-рые могут связать существ.
часть атомов того или иного элемента и тем самым повлиять на равновесное содержание
др. соединений.
-
"фиктивное" давление элемента j, т. е. то парциальное давление
соответствующих свободных атомов, к-рое имело бы место при полной диссоциации
всех содержащих данный элемент молекул. С помощью соответствующих констант диссоциации
давление рi в ур-ниях (4) может быть выражено через парциальные
давления рj составляющих элементов, находящихся в свободноатомном
состоянии. В результате из (4) получим систему нелинейных алгебраич. ур-ний
для pj. Определив из этой системы все pj, можно
вычислить рi для любого интересующего нас сорта молекул, составляя
соответствующие ур-ния диссоциации (1). При расчётах Д. р. качественный состав
газовой смеси должен быть задан заранее, и от исследователя требуется определ.
интуиция, чтобы не упустить важных соединений, к-рые могут связать существ.
часть атомов того или иного элемента и тем самым повлиять на равновесное содержание
др. соединений.
Более общий метод нахождения
равновесного состава газовой смеси основан на том факте, что при равновесии
в заданных условиях достигает экстремума некрая термодинамич. функция. В особенно
часто встречающемся случае, когда равновесие осуществляется при постоянных
Т и р, минимизируется энергия Гиббса газовой смеси:
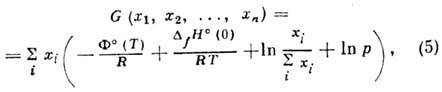
где п - число компонентов,
хi - число молей i-гo компонента в смеси. Для определения
равновесных значений xi необходимо найти минимум функции (5)
при условии баланса массы (4). Для решения этой задачи разработаны эффективные
вычислит. методы.
Методы, аналогичные изложенным,
позволяют исследовать и более общие случаи хим. равновесия, напр. определять
концентрации не только нейтральных, но и заряж. газов и кол-ва веществ в конденсиров.
фазах.
Расчёты Д. р. звёздных
атмосфер, выполняемые с кон. 20-х гг., позволили объяснить осн. характеристики
спектров холодных звёзд, в частности разделение спектральной последовательности
в области холодных звёзд на "кислородную" и "углеродную"
ветви (см. Спектральные классы ),особенности изменения интенсивности
молекулярных полос вдоль спектральной последовательности, различия молекулярных
спектров звёзд гигантов и карликов и др.

В. С. Стрельницкий
|
|