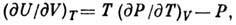
Джоуля закон - закон термодинамики, согласно к-рому внутренняя энергия идеального газа является
функцией одной лишь температуры и не зависит от объёма. Установлен экспериментально
Дж. П. Джоулем в 1845. Д. з. является следствием второго начала термодинамики. Из условия, что приращение энтропии есть полный дифференциал, следует для
производной внутр. энергии U по объёму V при пост. температуре T:
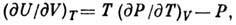
где P - давление.
Для идеального газа, удовлетворяющего ур-нию Клапейрона, PV=RT, где R - газовая постоянная, 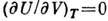 , это и есть Д. з. Степень справедливости Д. з. для газов малой плотности можно
оценить по величине Джоуля-Томсона эффекта. Для идеального газа эффект
отсутствует. Д. з. легко получить в кинетич. теории газов: поскольку в идеальном
газе отсутствует взаимодействие между молекулами, изменение расстояний между
ними (объёма) не меняет внутр. энергии.
, это и есть Д. з. Степень справедливости Д. з. для газов малой плотности можно
оценить по величине Джоуля-Томсона эффекта. Для идеального газа эффект
отсутствует. Д. з. легко получить в кинетич. теории газов: поскольку в идеальном
газе отсутствует взаимодействие между молекулами, изменение расстояний между
ними (объёма) не меняет внутр. энергии.

Д. H. Зубарев
Когда тот или иной физик использует понятие "физический вакуум", он либо не понимает абсурдности этого термина, либо лукавит, являясь скрытым или явным приверженцем релятивистской идеологии.
Понять абсурдность этого понятия легче всего обратившись к истокам его возникновения. Рождено оно было Полем Дираком в 1930-х, когда стало ясно, что отрицание эфира в чистом виде, как это делал великий математик, но посредственный физик Анри Пуанкаре, уже нельзя. Слишком много фактов противоречит этому.
Для защиты релятивизма Поль Дирак ввел афизическое и алогичное понятие отрицательной энергии, а затем и существование "моря" двух компенсирующих друг друга энергий в вакууме - положительной и отрицательной, а также "моря" компенсирующих друг друга частиц - виртуальных (то есть кажущихся) электронов и позитронов в вакууме.
Однако такая постановка является внутренне противоречивой (виртуальные частицы ненаблюдаемы и их по произволу можно считать в одном случае отсутствующими, а в другом - присутствующими) и противоречащей релятивизму (то есть отрицанию эфира, так как при наличии таких частиц в вакууме релятивизм уже просто невозможен). Подробнее читайте в FAQ по эфирной физике.
|
|